经内蒙古自治区药品检验研究院等5家药品检验机构检验,标示为江西九连山药业有限公司等14家企业生产的18批次药品不符合规定。
经内蒙古自治区药品检验研究院等5家药品检验机构检验,标示为江西九连山药业有限公司等14家企业生产的18批次药品不符合规定。现将相关情况通告如下:
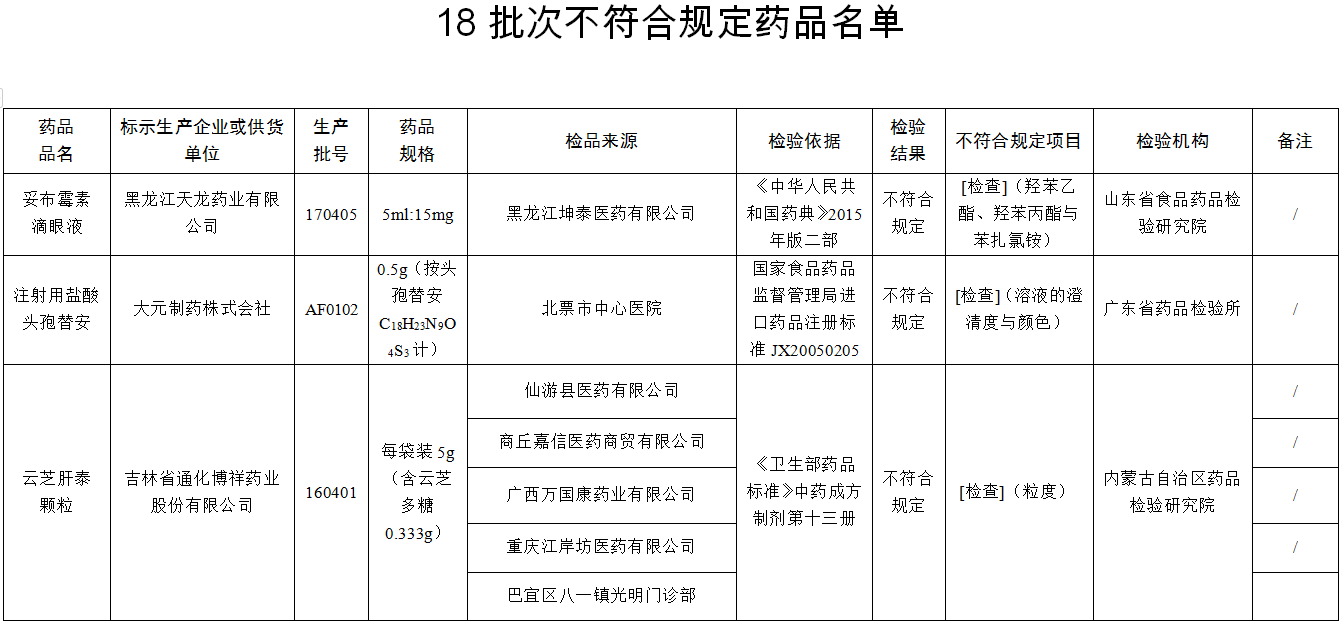
一、经山东省食品药品检验研究院检验,标示为黑龙江天龙药业有限公司生产的1批次妥布霉素滴眼液不符合规定,不符合规定项目为羟苯乙酯、羟苯丙酯与苯扎氯铵。
经广东省药品检验所检验,标示为大元制药株式会社生产的1批次注射用盐酸头孢替安不符合规定,不符合规定项目为溶液的澄清度与颜色。
经内蒙古自治区药品检验研究院检验,标示为吉林省通化博祥药业股份有限公司、江西九连山药业有限公司生产的5批次云芝肝泰颗粒不符合规定,不符合规定项目包括粒度、性状、含量测定。
经甘肃省药品检验研究院检验,标示为安国市辉发中药饮片加工有限公司、亳州市谯城区万事祥中药饮片有限公司等3家企业生产的3批次白芷不符合规定,不符合规定项目包括含量测定、二氧化硫残留量。
经安徽省食品药品检验研究院检验,标示为安国市安兴中药饮片有限公司、安国市久旺药业有限公司、河北仁心药业有限公司、云南宁坤生物科技有限公司、云南宗顺生物科技有限公司、昆明蓝海中药材饮片有限公司、新疆和济中药饮片有限公司生产的8批次槟榔不符合规定,不符合规定项目为黄曲霉毒素。(详见附件)
二、对上述不符合规定药品,相关药品监督管理部门已采取查封、扣押等控制措施,要求企业暂停销售使用、召回产品,并进行整改。
三、国家药品监督管理局要求相关省级药品监督管理部门对上述企业和单位依据《中华人民共和国药品管理法》第七十三、七十四、七十五条等规定对生产销售假劣药品的违法行为进行立案调查,自收到检验报告书之日起3个月内完成对相关企业或单位的调查处理并公开处理结果。
特此通告。
国家药监局
2018年12月24日


声明:本文系药智网转载内容,版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请与本网站留言联系,我们将在第一时间删除内容!

















